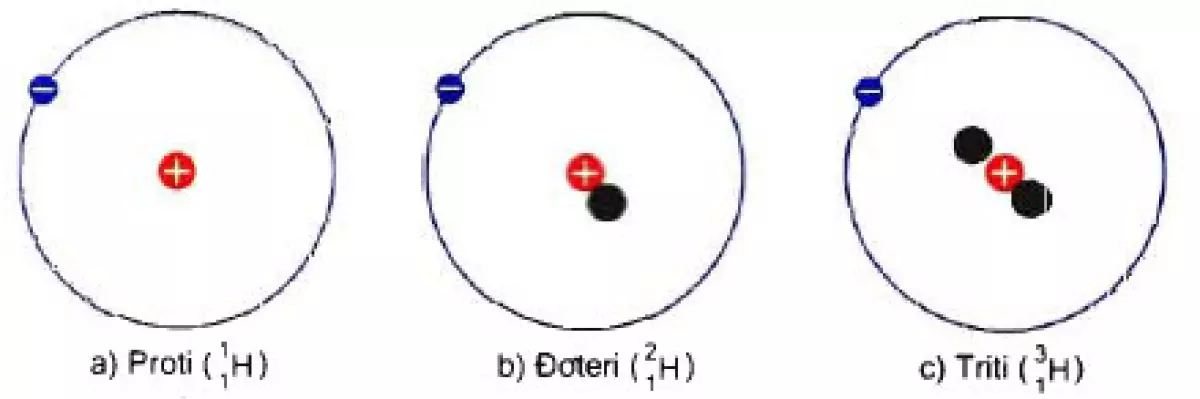
 Hình 1: Sơ đồ cấu tạo nguyên tử ba đồng vị của nguyên tố Hidro
Hình 1: Sơ đồ cấu tạo nguyên tử ba đồng vị của nguyên tố Hidro
Giới thiệu Trong bài viết này, chúng ta sẽ tìm hiểu về số khối là gì, số hiệu nguyên tử là gì, cách tính số khối, công thức và nguyên tử khối trung bình. Bài viết sẽ giúp các bạn hiểu rõ hơn về các khái niệm này và cách áp dụng chúng trong hóa học.
1. Hạt nhân nguyên tử
1.1 Điện tích hạt nhân
- Hạt nhân của một nguyên tử gồm các hạt proton và nơtron. Số proton trong hạt nhân được ký hiệu là Z và điện tích của hạt nhân bằng Z+.
- Số proton trong hạt nhân cũng bằng số electron của nguyên tử, vì nguyên tử trung hòa về điện. Vì vậy, số đơn vị điện tích hạt nhân Z cũng bằng số proton (p) và số electron (e) của nguyên tử.
1.2 Số khối và công thức tính số khối
- Số khối (A) của hạt nhân là tổng số proton (Z) và số nơtron (N) có trong hạt nhân đó: A = Z + N.
2. Nguyên tố hóa học
2.1 Định nghĩa và tính chất của nguyên tố hóa học
- Nguyên tố hóa học là những nguyên tử có cùng điện tích hạt nhân.
- Các nguyên tử thuộc cùng một nguyên tố hóa học có cùng số proton và cùng số electron, do đó có tính chất hóa học giống nhau.
- Hiện nay, có khoảng 92 nguyên tố hóa học tồn tại trong tự nhiên và khoảng 18 nguyên tố nhân tạo được tổng hợp trong các phòng thí nghiệm hạt nhân.
2.2 Số hiệu nguyên tử và ký hiệu nguyên tử
- Số hiệu nguyên tử (Z) của một nguyên tố là số đơn vị điện tích hạt nhân nguyên tử của nguyên tố đó.
- Ký hiệu nguyên tử được ghi bằng cách đặt số khối (A) ở bên trên, số hiệu nguyên tử (Z) ở bên dưới ký hiệu nguyên tố X. Ví dụ: X(A, Z).
- Số hiệu nguyên tử (Z) cung cấp thông tin về số proton và số electron trong nguyên tử. Nếu biết số khối (A) và số hiệu nguyên tử (Z), ta có thể tính được số proton và số nơtron (N = A - Z) trong hạt nhân nguyên tử và số electron của nguyên tử đó.
- Ví dụ: Đối với nguyên tố Natri (Na), số khối A = 23 và số hiệu nguyên tử Z = 11. Vậy trong hạt nhân nguyên tử Na có 11 proton và vỏ nguyên tử Na có 11 electron. Số nơtron (N) trong hạt nhân là 12 (12 = 23 - 11).
3. Đồng vị
- Các nguyên tử thuộc cùng một nguyên tố hóa học có thể có số khối khác nhau, vì hạt nhân của chúng có cùng số proton nhưng có thể có số nơtron khác nhau.
- Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có cùng số proton nhưng khác nhau về số nơtron. Vì vậy, số khối (A) của chúng khác nhau.
- Các đồng vị được xếp vào cùng một ô nguyên tố trong bảng tuần hoàn.
- Hiện nay đã biết tồn tại khoảng 340 đồng vị tự nhiên và hơn 2400 đồng vị nhân tạo được sử dụng trong y học và nông nghiệp.
4. Nguyên tử khối và nguyên tử khối trung bình
4.1 Nguyên tử khối
- Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó so với đơn vị khối lượng nguyên tử.
- Khối lượng của một nguyên tử bằng tổng khối lượng của proton, nơtron và electron trong nguyên tử, nhưng do khối lượng của electron quá nhỏ so với hạt nhân nên khối lượng của một nguyên tử coi như bằng khối lượng của hạt nhân nguyên tử.
- Đa số các nguyên tố hóa học là hỗn hợp của nhiều đồng vị với tỉ lệ phần trăm số nguyên tử xác định. Do đó, nguyên tử khối của các nguyên tố có nhiều đồng vị được tính là nguyên tử khối trung bình của hỗn hợp các đồng vị với tỉ lệ phần trăm số nguyên tử tương ứng.
Vậy là chúng ta đã tìm hiểu về số khối là gì, số hiệu nguyên tử, công thức và nguyên tử khối trung bình. Hiểu rõ các khái niệm này sẽ giúp chúng ta nắm bắt được cấu trúc và tính chất của các nguyên tử trong hóa học. Hy vọng bài viết đã giúp bạn thêm kiến thức!












