Hóa học là một môn học thú vị, nhưng đôi khi việc nhớ công thức và kiến thức có thể là một thách thức. Vì vậy, VietJack đã biên soạn một bài viết tóm tắt công thức Hóa học lớp 8 Chương 3 nhằm giúp bạn dễ dàng hơn trong việc nhớ kiến thức quan trọng.
Công Thức Tính Số Mol
- Công thức này áp dụng cho tính số mol khí ở điều kiện tiêu chuẩn.
- Công thức này cũng áp dụng cho tính số mol khí ở điều kiện nhiệt độ phòng.
- Nếu bạn muốn tính số mol chất khí trong các điều kiện khác, chỉ cần thay đổi các giá trị áp suất, thể tích và nhiệt độ trong công thức.
Công Thức Tính Tỉ Khối Chất Khí
- Tỉ khối của chất A so với chất B có thể được tính bằng công thức tương ứng.
- Tỉ khối của chất A so với không khí cũng có công thức riêng của nó.
Công Thức Tính Khối Lượng Chất Tan
- Để tính khối lượng chất tan, sử dụng công thức tương ứng và nhập các giá trị số phù hợp.
- Nếu bạn muốn tính nồng độ phần trăm, chỉ cần thay đổi giá trị nồng độ và khối lượng dung dịch trong công thức.
Công Thức Tính Thể Tích Chất Khí
- Để tính thể tích khí ở các điều kiện tiêu chuẩn và nhiệt độ phòng, sử dụng các công thức tương ứng.
- Nếu bạn muốn tính thể tích khí ở các điều kiện khác, chỉ cần thay đổi giá trị áp suất, nhiệt độ và số mol trong công thức.
Công Thức Tính Thành Phần Phần Trăm Về Khối Lượng
- Đối với hỗn hợp gồm hai chất A và B, bạn có thể tính khối lượng hỗn hợp và các thành phần phần trăm tương ứng.
- Đối với chất khí, tỉ lệ thể tích chính là tỉ lệ số mol, cho phép tính toán dễ dàng hơn.
Công Thức Tính Hiệu Suất Phản Ứng
- Hiệu suất phản ứng có thể được tính bằng khối lượng sản phẩm thực tế so với khối lượng lý thuyết.
- Bạn cũng có thể tính hiệu suất phản ứng dựa trên số mol chất tham gia.
Công Thức Tính Khối Lượng Chất Tham Gia và Sản Phẩm Khi Có Hiệu Suất
- Khi có hiệu suất phản ứng nhỏ hơn 100%, lượng chất tham gia và sản phẩm thực tế thu được sẽ khác so với lý thuyết.
- Công thức sẽ giúp tính toán khối lượng chất tham gia và sản phẩm khi có hiệu suất.
Công Thức Tính Thành Phần Phần Trăm Về Khối Lượng Các Nguyên Tố Trong Hợp Chất
- Với công thức hóa học đã biết, bạn có thể tính được tỷ lệ phần trăm của các nguyên tố trong hợp chất.
Tóm tắt công thức Hóa học lớp 8 Chương 3 này sẽ giúp bạn hiểu và nhớ lâu hơn kiến thức quan trọng. Hãy áp dụng chúng vào việc học và thực hành để trở nên thành thạo hơn trong môn học này.
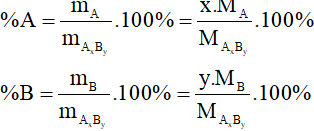 Hình ảnh minh họa
Hình ảnh minh họa
Nếu bạn muốn tìm hiểu thêm về các chương khác trong môn Hóa học lớp 8, hãy tham khảo các bài viết tóm tắt khác trên VietJack.
Săn SALE shopee Tết:
- Đồ dùng học tập giá rẻ
- Sữa dưỡng thể Vaseline chỉ hơn 40k/chai
- Tsubaki 199k/3 chai
- L'Oreal mua 1 tặng 3















